BRASÍLIA — A pandemia tem dado um pouco de trégua nas últimas semanas, mas os cuidados com a infecção pelo coronavírus não podem arrefecer e deverão permanecer por muitos e muitos meses. Ainda assim, o Ministério da Saúde ignora medicamentos, coquetéis e associações de anticorpos que podem ajudar no tratamento. Um ano após a aprovação na Agência Nacional de Vigilância Sanitária (Anvisa) do primeiro remédio para a Covid-19, nenhum está disponível na rede pública.
A pasta planeja rediscutir o tema em reunião interna nesta segunda-feira. Só depois a Comissão Nacional de Incorporação de Tecnologias no Sistema Único de Saúde (Conitec), responsável por definir tratamentos oferecidos pelo SUS, deve voltar a debater a indicação.
A Anvisa já concedeu autorização de uso emergencial a sete medicamentos, que incluem anticorpos monoclonais e associação de anticorpos. Porém, suspendeu o aval do banlanivimabe + etesevimabe, da Eli Lilly, em fevereiro, já que a empresa não entregou dados de eficácia contra a Ômicron.
No último protocolo, a Conitec avalia que o benefício dessas terapias não justifica a indicação devido a critérios de “alto custo, baixa experiência de uso, incertezas em relação à efetividade e a sua indisponibilidade no sistema de saúde”. A indicação pode mudar a partir das novas reuniões.
— Como é um pequeno número de pacientes, não vai onerar o governo — afirma o professor de Imunologia do Instituto de Ciências Biomédicas da Universidade de São Paulo (ICB-USP) Antônio Condino Neto. — Se pacientes imunodeprimidos que não conseguiram se beneficiar da vacina como deveriam tivessem acesso a esses medicamentos, é claro que mortes poderiam ter sido evitadas.
Na mira do governo para possíveis aquisições, está o Evusheld, a mais recente aprovação da Anvisa e desenvolvido pela AstraZeneca a partir de anticorpos humanos. É o primeiro tratamento que pode prevenir a infecção por coronavírus. A indicação do laboratório se dá para imunodeprimidos a partir de 12 anos. Ao GLOBO, a empresa confirmou o diálogo com o governo federal, mas não forneceu previsões de quantidade e de data de entrega. Os Estados Unidos, por sua vez, têm acordo para 1,7 milhões de doses.
Médicos ouvidos pelo GLOBO destacam a importância de o país investir nos medicamentos e terapias para a Covid-19. Para o professor de Medicina da Universidade Federal de Mato Grosso do Sul (UFMS) e pesquisador da Fundação Oswaldo Cruz (Fiocruz) Julio Croda, é “inadequado” que o ministério não tenha incorporado os remédios até o momento, o que vai na contramão de outros países como os Estados Unidos.
— São supernecessários, principalmente para pessoas com maior risco. Se tivéssemos medicações sendo distribuídas gratuitamente, como os Estados Unidos estão propondo nas farmácias, poderíamos utilizar na população geral ou em grupos de risco, com comorbidades, imunossuprimidos e idosos — pontua o infectologista.
Apesar do avanço da vacinação ter ajudado a diminuir as internações e mortes por Covid-19 de forma ampla, grupos específicos podem se beneficiar de uma alternativa a mais no enfrentamento da doença, tais como os imunossuprimidos — pacientes com câncer, HIV ou aids e transplantados, por exemplo — e idosos, apontam especialistas.
— Seria bom que o Brasil incorporasse essas medicações. Agora, a gente não vê esse debate acontecer dentro do ministério. A Anvisa está aprovando algumas medicações, mas também de forma lenta. Isso precisa ser acelerado, precisa ser avaliado na Conitec. A gente não tem protocolo de atenção à saúde dos pacientes com Covid-19, de tratamento ambulatorial ou hospitalar — critica Croda, ex-diretor de Vigilância em Saúde do ministério.
Interlocutores ligados à Conitec afirmaram ao GLOBO que a discussão sobre o uso de antivirais e imunobiológicos só deve voltar à mesa depois que o ministro da Saúde, Marcelo Queiroga, decidir a respeito de protocolos anteriores. No último, ao comitê também contraindicou o uso do ‘kit Covid’ — com medicamentos ineficazes contra a doença, como cloroquina, hidroxicloroquina, ivermectina e azitromicina.
A recomendação foi barrada pelo então secretário de Ciência, Tecnologia, Inovação e Insumos Estratégicos (SCTIE), Hélio Angotti Neto. Cientistas elaboraram recurso contra a decisão, já negado pelo oftalmologista, que é olavista declarado. O caso subiu à instância final: o gabinete de Queiroga.
— O que fica evidente para nós, cidadãos, é que existem forças dentro do Ministério da Saúde pró-adoção de medicamentos como a cloroquina e a ivermectina, que comprovadamente não trazem benefício ao tratamento. É uma lástima, porque não funcionam. É desperdício de dinheiro — argumenta Condino Neto, que preside o Departamento de Imunologia da Sociedade Brasileira de Pediatria (SBP).
Um dos medicamentos aprovados pela Anvisa, o REGN-COV2, formado por Casirivimabe e Indevimabe, teve parecer da fabricante, a Roche, em dezembro, atestando que o produto “não mantém atividade neutralizante contra a variante Ômicron”. Assim como em outros, não houve evolução na negociação com o ministério. Já o Paxlovid, da Pfizer, está sob análise da Anvisa desde o mês passado. Segundo o laboratório, a expectativa é produzir de 80 milhões a 120 milhões de doses neste ano.
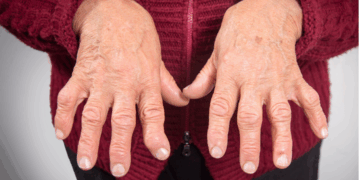
Procurada pelo GLOBO, a Anvisa informou que “não é possível antecipar futuras autorizações ou cancelamentos. Além disso, tivemos o pedido de registro do Remdesivir (não é uso emergencial) e a aprovação da nova indicação para o Baracitinibe”, diz a nota. Esse medicamento é usado contra artrite reumatoide.
Em nota, o Ministério da Saúde informou que “tem realizado reuniões com indústrias farmacêuticas, a fim de orientar as submissões de tecnologias” para incorporação ao SUS. Até o momento, segundo a pasta, seis tecnologias foram analisadas pela Conitec.
O ministério destacou que a recomendação final foi pela não incorporação do remdesivir, do indevimabe e casirivimabe (avaliada em duas ocasiões e, em ambas, com recomendação desfavorável), do regdanvimabe (por descumprimento de requisitos legais). Não houve pedido para submissão do sotrovimabe e o processo sobre o baricitinibe está em análise, disse a pasta.
Fonte: O Globo.