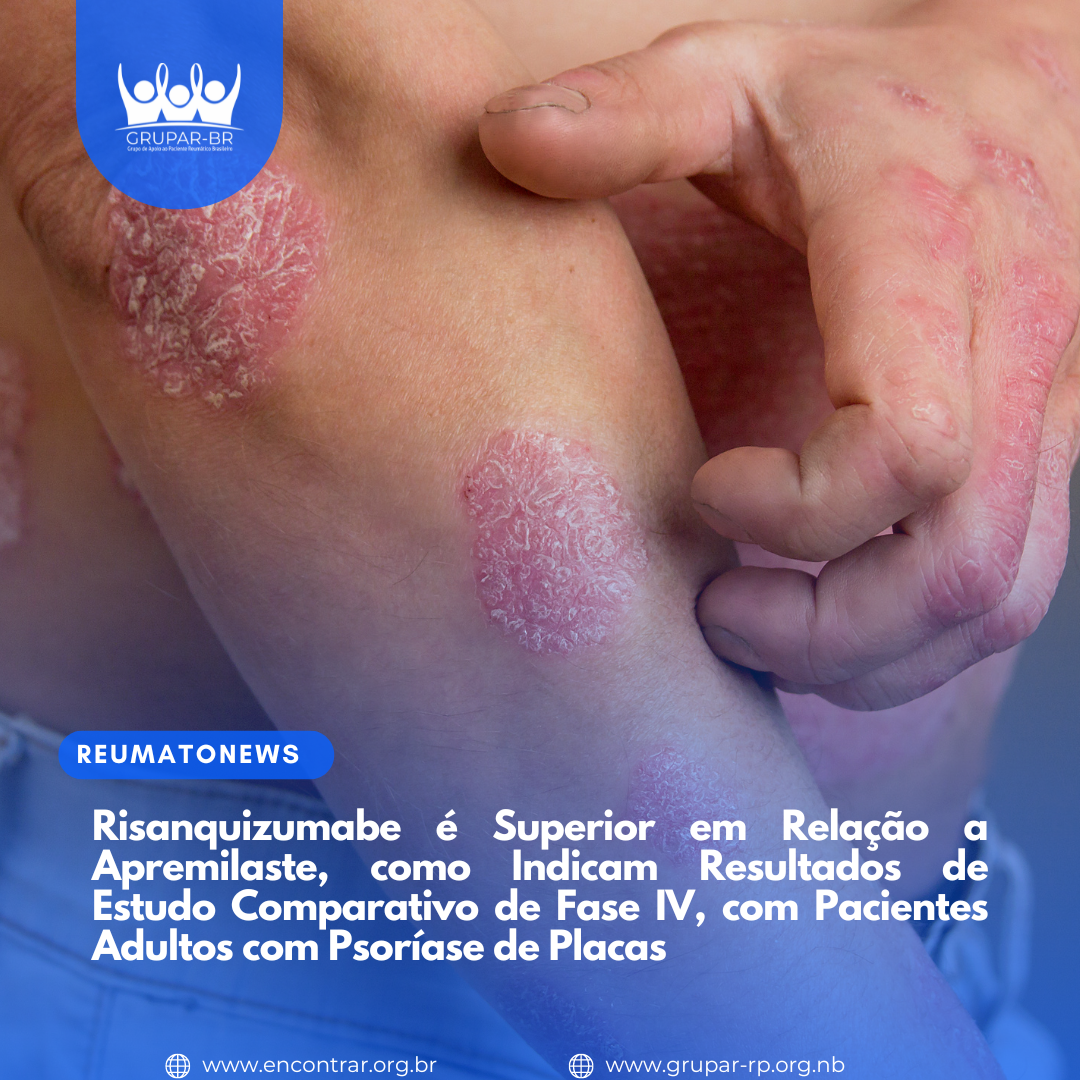
São Paulo, 04 de agosto de 2023 — A AbbVie (NYSE: ABBV) anunciou (26/07/2023) que o periódico científico British Journal of Dermatology publicou os resultados do estudo comparativo de Fase 4 IMMpulse, que avaliou a eficácia e a segurança de risanquizumabe, em comparação com apremilaste, no tratamento de pacientes adultos com psoríase em placas moderada e elegíveis a terapia sistêmica1. Foram alcançados todos os desfechos primários e secundários estabelecidos para o estudo, sem que novos sinais de segurança tenham sido identificados1.
“Este estudo destaca a eficácia de risanquizumabe, em comparação a apremilaste, contribuindo para que mais pacientes elegíveis para tratamento sistêmico alcançassem altos níveis de cicatrização das lesões da pele, e também reforça o perfil de segurança observado em estudos anteriores”, disse o médico Mudra Kapoor, vice-presidente de Assuntos Médicos Globais em Imunologia da AbbVie. “Esses dados comparativos são cruciais para ajudar os pacientes e seus médicos a tomar decisões sobre o tratamento de doenças, com base nas evidências que corroboram o uso de risanquizumabe como uma opção de tratamento para adultos que vivem com psoríase moderada”.
Os destaques deste estudo aberto e cego incluem:
- Na semana 16, uma proporção significativamente maior de pacientes que receberam risanquizumabe alcançou os desfechos co-primários do período A, de PASI 90 e sPGA 0/1 (55,9%, isto é 66 em 118 dos pacientes atingiram PASI 90 e 75,4%, isto é 89 em 118 atingiram sPGA 0/1 com risanquizumabe), versus 5,1% (12/234) e 18,4% (43/234) com apremilaste e ambos com P<0,001]1.
- A proporção de pacientes que atingiram o desfecho secundário de PASI 75 na semana 16 também foi significativamente maior entre aqueles tratados com risanquizumabe em comparação aos pacientes que receberam apremilaste (84,7%, 100/118, versus 18,8% 44/234, respectivamente; P<0,001)1
- Na semana 52, entre os pacientes que falharam em atingir PASI 75 após 16 semanas de tratamento com apremilaste, uma proporção significativamente maior de pacientes randomizados novamente para tratamento com risanquizumabe alcançou o desfecho primário de PASI 90 do Período B, em comparação com aqueles re-randomizados em continuar o tratamento com apremilaste (72,3%, 60/83, versus 2,6%,2/78; P<0,001)1.
- Após 52 semanas de tratamento contínuo, 73,7% dos pacientes com risanquizumabe atingiram os desfechos PASI 90 e 63,6% PASI 100, enquanto, com apremilaste, 4,5% e 2,7% dos pacientes atingiram a mesma pontuação de PASI 90 e PASI 100 na semana 52, respectivamente (nominal p-valor <0,001 para ambas as comparações).
O perfil de segurança de risanquizumabe neste estudo foi consistente com estudos relatados anteriormente; foi bem tolerado sem identificação de novos sinais de segurança1. Os eventos adversos mais frequentes (relatados em ≥5%) em pacientes tratados com risanquizumabe foram COVID-19, nasofaringite e infecção do trato respiratório superior1. Diarreia, náusea e dor de cabeça foram os mais frequentes entre pacientes tratados com apremilaste1. Eventos adversos graves foram relatados em 0,8% e 2,9% dos pacientes tratados com risanquizumabe e 1,7% e 2,1% dos pacientes tratados com apremilaste nos Períodos A e B, respectivamente1.
“Como médica, é crucial validar diferentes opções que podem atingir altos objetivos de tratamento. Este estudo fornece dados relevantes para a prática médica”, disse a pesquisadora principal do estudo, a médica Linda Stein Gold, diretora de Pesquisa Clínica, do departamento de dermatologia, do Sistema de Saúde Henry Ford. “Esses dados reforçam a eficácia de risanquizumabe para uso em pacientes com psoríase moderada elegíveis ao uso sistêmico, sendo que seu perfil de segurança, neste estudo, é semelhante a estudos anteriores”.
Com base nas análises do TSQM-9, os pacientes tratados com risanquizumabe relataram maior satisfação com o tratamento na semana 16, com pontuações mais altas em todos os três domínios de satisfação – eficácia (80,6), conveniência (84,9) e satisfação geral (86,2) – em comparação com pacientes tratados com apremilaste (46,9, 69,0 e 47,7, respectivamente; valor-p nominal <0,001 para todas as comparações)1.
Risanquizumabe faz parte de uma colaboração entre a Boehringer Ingelheim e a AbbVie, com a AbbVie liderando o desenvolvimento e a comercialização globalmente.
As indicações de risanquizumabe aprovadas no Brasil podem ser conhecidas em sua bula7.
Sobre a psoríase
A psoríase é uma condição inflamatória crônica da pele, mediada pelo sistema imunológico, que produz espessamento e descamação da pele devido ao rápido crescimento das células da pele2. Afeta cerca de 2-3% das pessoas em todo o mundo3. A psoríase também afeta aspectos emocionais e sociais de quem convive com doença, contribuindo para a redução da qualidade de vida dos pacientes.
Fonte: Assessoria de Imprensa